|
首頁 >> 醫藥行銷師(MR)專區 >> 醫藥行銷倫理規範
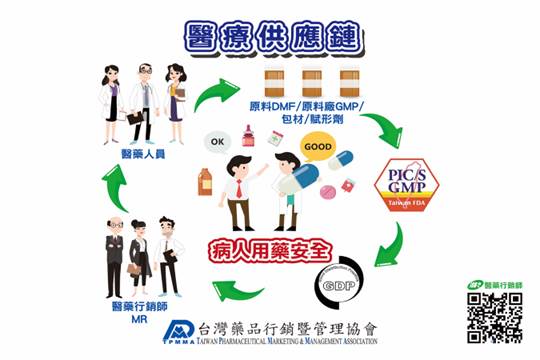
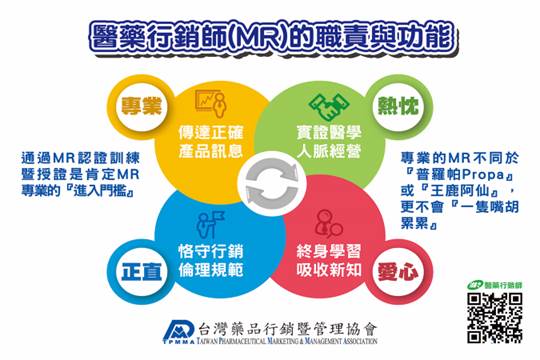
李勝文整理 2020年6月30日 醫藥行銷師(MR)在整體醫療供應鏈上為了確保病人用藥安全扮演非常重要腳色 醫藥行銷師(MR)需具備四大特色:(1)專業 (2)熱忱 (3)愛心 (4)正直
醫藥行銷師(MR)四大信念 醫藥行銷師(MR)於通過認證訓練取得醫藥行銷師(MR)資格時,應集體宣讀醫藥行銷師(MR)誓詞同時親自簽名,誓詞留存於台灣藥品行銷暨管理協會(TPMMA)以示負責。
醫藥行銷師認證制度 台灣醫藥行銷師認證制度於1995年由中華民國藥品行銷暨管理協會之傑出藥品專業經理聯誼會所推動,其目的為提升藥品行銷人員素質,增進整體醫療品質,保障國人身體健康,並期望藉由 MR 認證制度的推展,樹立完善的醫藥行銷倫理,建立世界水準的醫藥行銷體制,提升國家形象與競爭力。 我國食品藥物管理署 (Taiwan Food and Drug Administration;TFDA) 以守護飲食用藥安全、引領科技全新紀元、創造安心消費環境為使命,並以捍衛全民健康、邁向食品藥物管理新紀元為願景,強調打造一個藥求安全,食在安心的健康台灣新環境。用藥安全是政府施政的使命,與用藥安全相關的每一個環節實不容忽視。 藥物安全監視 (Pharmacovigilance),以確保民眾用藥安全是世界潮流,也是先進國家永遠追求的目標,更是 TFDA 施政的使命。硬體與軟體必須兼備、缺一不可,硬體管理方面,原料主檔案 (Drug Master File;DMF)、原料廠實施優良製造規範 (Good Manufacturing Practice;GMP)、包材、賦形劑,國際醫藥品稽查協約組織藥品優良製造規範 (Pharmaceutical Inspection Co-operation Scheme/Good Manufacturing Practice;PIC/S GMP),藥品優良運銷規範 (Good Distribution Practice;GDP) 等已具備,但是軟體監督如醫藥行銷師的資格認定,藥事法第33條已不合時宜、落伍了,醫療供應鏈必須環環緊密相扣,不可鬆動。 醫藥行銷師(MR)認證制度的推動,歷年來受到衛生主管機關包括衛生福利部,食藥署、健保署,縣市衛生局與醫療院所等認同並多方協助,單位主管均親臨擔任認證訓練講師,表示對醫藥行銷師(MR)認證制度肯定與支持。目前我國之 MR 認證證照屬於個人資格且是業界自主,由 TPMMA 頒發。取得醫藥行銷師(MR)認證後6年內需接受120小時之持續教育,才能持續保有 MR 資格。醫藥行銷師(MR)認證制度截至2018年底已有2,787位醫藥專業行銷人員取得 MR 認證資格。 醫藥行銷倫理規範之重要性
重要醫藥行銷倫理規範收載如下: IRPMA市場行銷規範(COP) IRPMA行為與產品行銷倫理指導原則 2012年IRPMA市場行銷規範之訂定,乃以下列指導原則為基準。所有IRPMA會員公司及其代理商皆應遵守IRPMA市場行銷規範,以確保與所有相關單位的正當互動。 檔案下載 2003年藥業營運規範(COBO)草案
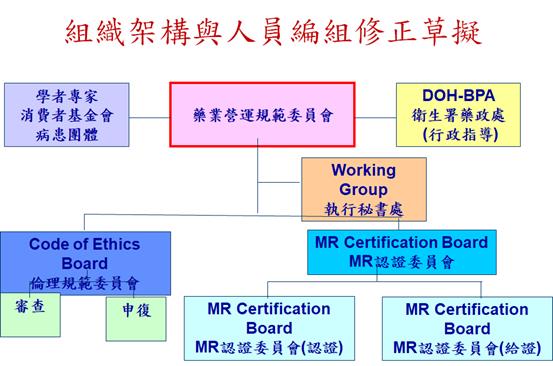
2. 藥業營運規範(COBO)參與機構及公協會
3. 藥業營運規範(COBO) - 推廣(MR)認證及Code of Ethics企畫案共同研究單位代表
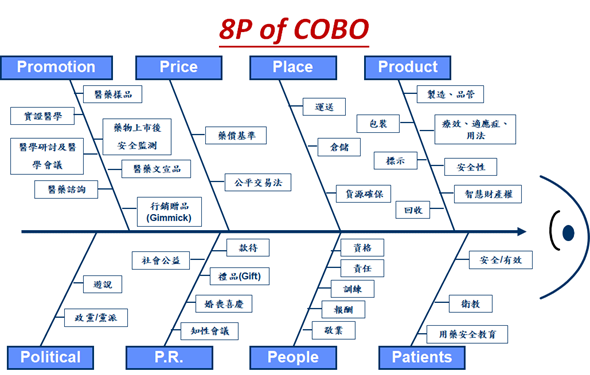
4. 藥業營運規範(COBO)設立目的
5. 藥業營運規範(COBO)涵蓋範圍 藥業營運規範(COBO)準則條文 公務員廉政倫理規範 醫界倫理紀律宣言 墨西哥市原則(The Mexico City Principles) 吉隆坡原則(The Kuala Lumpur Principles) |
 MR教育訓練-訓練課程
MR教育訓練-訓練課程